Informationen für Kollegen
Osteoporose, eine häufige Erkrankung
Epidemiologie
Osteoporose ist eine systemische Skeletterkrankung, die mit reduzierter Knochenmasse und aufgelockerter Mikroarchitektur einhergeht. Daraus folgt eine erhöhte Frakturrate. Da Osteoporose eine starke Altersabhängigkeit zeigt, führt die demographische Entwicklung zu einer Zunahme der Inzidenz. Nach Ergebnissen der Bone Evaluation Study (BEST) sind ca. 5,6 Millionen Patienten in Deutschland betroffen (Frauen: 4,8 Mio.; Männer: 849.000). Dies entspricht einer Prävalenz von 17%. Es ist ein starker Altersanstieg zu beobachten (50–54 Jahre: 6%; >74 Jahre 34%). Die Inzidenz lag im Jahr 2009 bei 1,9%; dies ergibt eine Neuerkrankungsrate von 768.000 Menschen jährlich. Hinzu kommen Patienten, die osteoporosebedingte Frakturen erlitten haben und nicht diagnostiziert wurden.
Die jährliche Mortalität liegt bei 2%. Die Osteoporose ist in Deutschland eine der bedeutendsten Volkskrankheiten.
Osteoporose ist eine multifaktorielle Erkrankung. Von der primären Osteoporose werden sekundäre Formen unterschieden. Durch die unterschiedliche Knochenarchitektur und den postmenopausalen Östrogenverlust mit nachfolgendem Anstieg der Knochenresorption sind zu etwa 80 % Frauen erkrankt, daher der Begriff der „postmenopausalen Osteoporose“. Sind bereits eine oder mehrere Frakturen als Folge der Osteoporose aufgetreten, spricht man von manifester Osteoporose.
Diagnostik
Die Diagnostik der Osteoporose umfasst zunächst eine Anamneseerhebung, die auf Abklärung von sekundären Ursachen und Risikofaktoren abzielt. Auch wenn sekundäre Faktoren nur bei 5-10% aller weiblichen und 50-60% aller männlichen Patienten für die Erkrankung verantwortlich sind, sollten sie immer ausgeschlossen werden. Es gibt eine Vielzahl bekannter Risikofaktoren, die eine Osteoporose begünstigen können. Dazu gehören nicht beeinflussbare Risikoparameter wie Geschlecht, eine positive Familienanamnese und das Lebensalter, aber auch „Life style Faktoren“ wie Nikotin, Bewegung, Ernährung und Alkoholkonsum. Bestimmte Krankheiten gehen mit einem hohen Risiko für eine Osteoporose einher. Dazu gehört die Hyperthyreose, chron. Darmerkrankungen, rheumatoide Arthritis und M. Parkinson. Bestimmte Medikamente wie z. B. Steroide, Antiepileptika, Aromatase-Hemmer bzw. Antiandrogene und - bei Überdosierung- Schilddrüsen-Hormone korrelieren ebenfalls mit einem erhöhten Fraktur Risiko. Die DVO Leitlinien werden regelmäßig überarbeitet und haben diese Risikofaktoren tabellarisch zusammengefasst:
http://dv-osteologie.org/uploads/Leitlinie%202017/DVO%20Leitlinie_Kitteltaschenversion_gesamt.pdf
Das Frakturrisiko wird vom Lebensalter mitbestimmt. Mit jeder Dekade verdoppelt sich in etwa das Frakturrisiko. Wirbelkörperfrakturen sind neben dem Lebensalter der größte unabhängige Risikofaktor für zukünftige Knochenbrüche. Dies gilt sowohl für klinisch manifeste Wirbelkörperfrakturen, als auch für Wirbelkörperfrakturen, die als Zufallsbefund erkannt werden.
Die körperliche Untersuchung umfasst die Bestimmung der Körpergröße, bzw. den Größenverlust und das Körpergewicht. Dabei ist ein BMI < 20 ein eigener Risikofaktor. Bei einem Größenverlust von mehr als 5 cm besteht der Verdacht auf Wirbelkörperfrakturen. Typische Osteoporose Zeichen sind das „Tannenbaumphänomen“ der Haut des Rückens, ein verringerter Rippen-Becken-Abstand, eine Vergrößerung des Finger-Boden-Abstandes und Wirbelsäulenklopfschmerz oder Thorax Kompressionsschmerz (vor allem nach frischen Frakturen). Die Untersuchung der Mobilität, bzw. des Sturzrisikos ist einfach. Dem Kliniker stehen mit dem Einbeinstand, dem Chair-rising- dem Time-up-and-go- oder dem Tandemstand- Test einfache Instrumente zur Bestimmung des Sturzrisikos zur Verfügung.
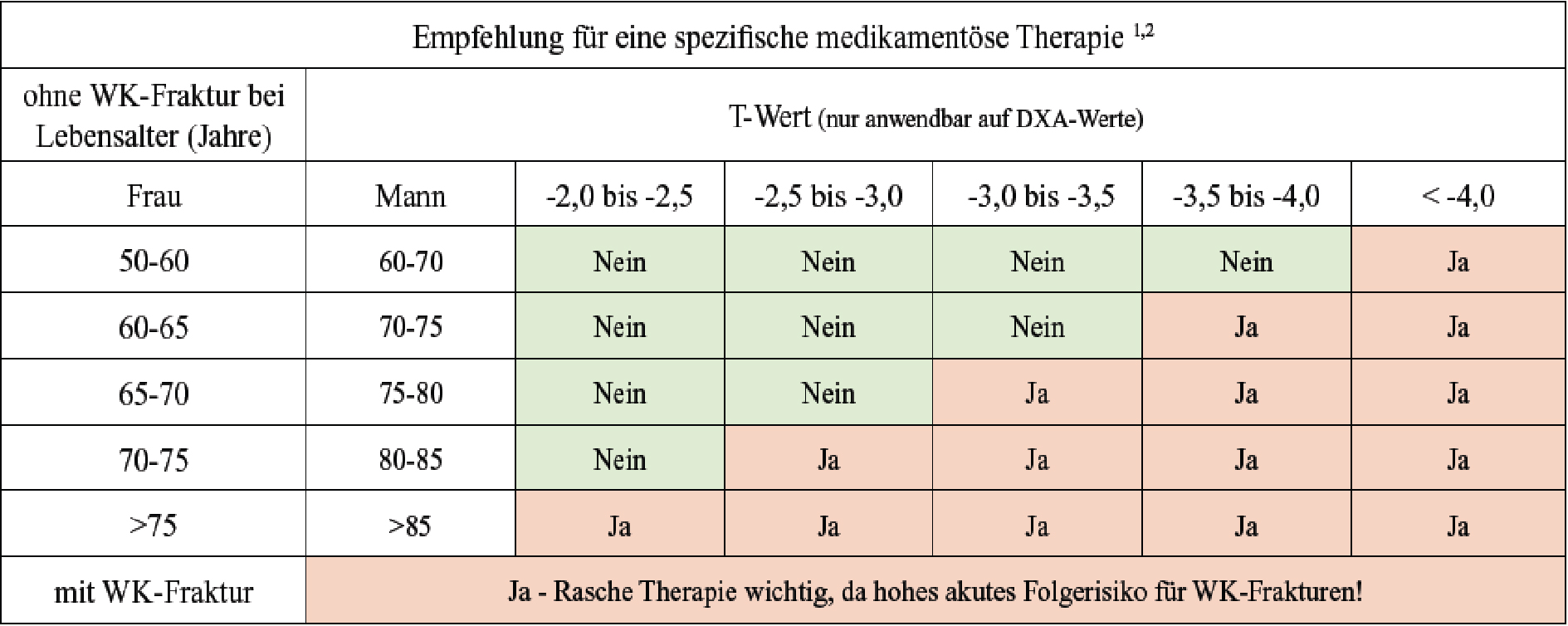
Die niedrige Knochendichte muss als unabhängiger Risikoparameter, nicht als Diagnose, interpretiert werden. Erst bei dem Verdacht auf Osteoporose, bzw. beim Vorhandensein von Risikofaktoren ist eine Untersuchung sinnvoll, zusätzlich bei allen Frauen ab 70 und allen Männern ab 80 Jahren. Nach DVO ist der Goldstandard die „Dual energy X-ray Absorptiometry“ (DXA) Messung. Der Wert wird im Vergleich zur gesunden 30jährigen Bevölkerung in Standardabweichungen (T-score) angeben. Laut WHO ist ein T-score von < -2,5 gleichbedeutend mit einer Osteoporose. Die DVO Leitlinien empfehlen nicht bei jeder vorhandenen Osteoporose eine spezifische Therapie. Erst wenn das Risiko > 30% ist, innerhalb der nächsten 10 Jahre eine Fraktur zu erleiden, sollte eine Therapie erfolgen. Diese Empfehlungen gelten nur für die Leitlinien des DVO (D-A-CH). In den angelsächsischen Ländern wird teilweise ab einem Frakturrisiko >20% therapiert. Da das Frakturrisiko mit höherem Lebensalter ansteigt, geben die Leitlinien abhängig vom Lebensalter, Geschlecht, Vorhandensein von Risikofaktoren und prävalenten Frakturen unterschiedliche Therapieempfehlungen. Steht neben der DXA Untersuchung die Bestimmung des „trabecular bone score“ (TBS) zur Verfügung, sollte dieser in die Einschätzung des Frakturrisikos mit einbezogen werden.
Auch wenn andere Methoden der Knochendichtemessung nicht oder nicht mehr als Standardmethode eingesetzt werden, verdienen sie doch eine Erwähnung. Aufgrund der relativ hohen Strahlenbelastung und der mäßigen Reproduzierbarkeit wird die QCT Messung der LWS nur noch als Verlaufskontrolle und nicht zur Primärdiagnostik empfohlen. Eine Ultraschallmessung (QUS) ist keine Knochendichtemessung im eigentlichen Sinne. Bei pathologischem Befund sollte auf jeden Fall eine DXA Messung folgen. Das HR-pQCT (XTreme CT®) ist eine gut etablierte, hochauflösende, strahlungsarme Methode zur Darstellung von Dichtewerten und Knochenstrukturen an Radius und Tibia in einer Auflösung von 80µm. Dadurch können, ähnlich wie bei einer Biopsie, Veränderung des Knochens erfasst werden, die bei einer reinen Dichtemessung nicht erkannt werden. Aufgrund der komplexen Ergebnisse gehört diese Methode in die Hand ausgewählter Spezialisten.
Bei Verdacht auf Wirbelfrakturen ist eine Röntgenuntersuchung der Brust- und Lendenwirbelsäule sinnvoll oder als Alternative die mit dem DXA Gerät durchgeführte sogenannte IVA/VFA Messung der lateralen Wirbelsäule.
Laboruntersuchungen sind bei der primären Osteoporose typischerweise unauffällig, sie dienen in erster Linie der Differentialdiagnostik. Die laut DVO Leitlinien empfohlenen Untersuchungen sind die Bestimmung von BSG/CRP, Blutbild, Kalzium, Phosphat, Natrium, Alkalische Phosphatase (AP), GGT, Kreatinin, TSH und die Eiweiß-Immunelektrophorese bzw. Immunelektrophorese. Bei Männern kann fakultativ das Testosteron mitbestimmt werden. In Einzelfällen ist die Bestimmung des Vitamin D und/oder der Knochenumbauparameter sinnvoll. Es gibt eine Vielzahl von Veröffentlichungen, die einen Einfluss der Knochenresoptionsmarker auf die Frakturrate nachweisen können. Der positive Einfluss des Vitamin D auf Knochenmasse, Muskelkraft und die Reduktion des Sturzrisikos ist gut dokumentiert. Andererseits leidet die Mehrheit der deutschen Bevölkerung an einem Vitamin D Mangel. Daher wird die Untersuchung des 25-OH Vitamin D gerade bei alten, gebrechlichen Patienten empfohlen.
Therapie
PrimärtherapieEine geringe Zufuhr von Kalzium führt zur Freisetzung von ossärem Kalzium. Eine Kalziumzufuhr von 1000 mg täglich mit der Nahrung wird als ausreichend angesehen. Nur bei geringerer Aufnahme empfehlen die Leitlinien eine Supplementierung. Dabei sollte die Gesamtzufuhr aus Nahrungskalzium und Supplementen 1500 mg nicht überschreiten, um einem erhöhten kardiovaskulärem Risiko vorzubeugen.
Serum-25-Hydroxy-Vitamin-D-Konzentrationen < 30 ng/ml bzw. 75 nmol/l liegen bei etwa 80 % der Bevölkerung vor. Unterhalb dieser Werte kann eine Steigerung der Knochenresorption beobachtet werden. Ein schwerer Vitamin-D-Mangel lässt sich in der Regel durch eine mindestens 30-minütige tägliche Sonnenlichtexposition von Gesicht und Armen unter optimalen Bedingungen vermeiden. Dabei sollte der Winkel der Sonneneinstrahlung > 35° sein. Dies ist in Deutschland nur von April bis Oktober der Fall. Die Leitlinien empfehlen daher eine Gabe von 800–1000 IE Vitamin D pro Tag oder einer aquivalenten Menge. Gerade ältere Patienten profitieren von einer Vitamin D Gabe, da bei einer Supplementierung von 800 IE Vitamin D täglich das Sturzrisiko signifikant reduziert werden kann.
Eine spezifische Therapie wird nach derzeitiger Evidenz bei Patienten mit 30%igem 10-Jahresfrakturrisiko begonnen. Nach frühestens einem Jahr Therapie kann eine Fraktursenkung erwartet werden. Da einige Präparate nur zeitlich begrenzt eingesetzt werden können und eventuell eine Therapieplanung für die nächsten 20-30 Jahre erforderlich ist, sollte vor Therapiebeginn eine grobe Planung der Sequenz erfolgen, um die Therapieeffekte bestmöglichst auszunutzen und mögliche Nebenwirkungen zu reduzieren.
Bisphosphonate sind die am häufigsten eingesetzten spezifischen Osteoporose Therapeutika. Die derzeit für die Osteoporose zugelassenen Bisphosphonate sind Alendronat, Risedronat, Ibandronat und Zoledronat. Dabei hat Ibandronat nicht die Zulassung für den Mann. Mittlerweile sind die ersten Bisphosphonate als Generika auf dem Markt. Bisphosphonate hemmen die Knochenresorption durch Hemmung des Enzyms Farnesylpyrophosphatase im reifen Osteoklasten. Die Verminderung des Knochenumbaus führt zu einer Verbesserung der Knochenarchitektur und zu einer Dichtezunahme. Die oralen Bisphosphonate werden mit 1-2% schlecht aus dem Gastrointestinaltrakt resorbiert, daher ist eine korrekte Einahme (mindestens 30 Minuten vor dem Frühstück mit Leitungswasser) wichtig. Bei der Anwendung von intravenösen Bisphosphonaten kommt es anfänglich zu sogenannten Akute Phasen Reaktionen mit Grippeähnlicher Symptomatik. Diese Symptome sind transient und ungefährlich. Eine seltene, aber häufig überschätzte Nebenwirkung ist die Osteonekrose des Kiefers (ONJ) mit einem Risiko von 1:10.000 in osteologischer Dosis. Mittlerweile sind auch viele positive Nebeneffekte der Bisphosphonate bekannt, wie eine Reduktion von kardiovaskulären Ereignissen, Malignomen und eine längere Verweildauer von Endoprothesen. Nach derzeitiger Evidenz sollen Bisphosphonate über 3-5 Jahre, je nach individuellem Risiko und klinischem Verlauf eingesetzt werden. Es kann nach Absetzen von einer Persistenz im Knochen und somit einem nachhaltigen Effekt ausgegangen werden.
Die selektiven Östrogen Rezeptor Modulatoren (SERMS), wie z. B. das Raloxifen imitieren die Östrogenwirkung auf den Knochen und erhalten einen physiologischen Knochenumbau. Sie bewirken, wie die Hormonersatz Therapie der postmenopausalen Frau, eine Hemmung der Knochenresorption indem sie die Osteoklastogenese durch Hemmung des RANK/RANK- Ligand Systems bremsen. Unter einer Therapie mit Raloxifen kommt es zu einer signifikanten Senkung des Auftretens klinischer vertebraler Frakturen. Die häufigsten Nebenwirkungen sind Hitzewallungen und Wadenkrämpfe. Zusätzlich hat Raloxifen die Zulassung in der Prävention des Mammakarzinoms. Kontraindikation sind bestehende oder in der Vorgeschichte aufgetretene Thromboembolien, da unter der Therapie die Inzidenz thromboembolischer Ereignisse erhöht ist. Selbstverständlich werden sie nur bei der postmenopausalen Frau eingesetzt.
Die Seit 2020 ist der neue Sklerostin Antikörper Romosozumab in der Therapie der schweren postmenopauselen Osteoporose mit hohem Frakturrisiko auf dem Markt. Romosozumab inhibiert die Knochenresorption und stimuliert gleichzeitig die Knochenformation durch Bindung und Inhibition von Sklerostin (dualer Wirkmechanismus). Dadurch kommt es zu einer schnellen Fraktursenkung und deutlicher Zunahme des Mineralgehaltes. Die Therapiedauer beträgt 12 Monate mit monatlichen Injektionen von 210 mg s.c. In einer Zulassungsstudie im Vergleich zu Alendronat traten gehäuft kardiovaskuläre Ereignisse auf. In den placebokontrollierten Studien war dies nicht der Fall. Trotzdem ist es bei anamnestisch bekanntem Apoplex oder Myokardinfarkt kontraindiziert. Aufgrund des ausgeprägten osteoanabolen Effektes und der Hypokalzämiegefahr muss auf eine ausreichende Kalziumzufuhr geachtet werden.
Denosumab ist der erste humane monoklonale Antikörper gegen RANKL. Dadurch wird der Knochenstoffwechsel auf der Ebene des Zytokinsystems beeinflusst. Durch Denosumab wird die Bildung der Osteoklasten aus Präosteoklasten gebremst. Die Anwendung erfolgt alle 6 Monate als subcutane Injektion. Es existieren sehr gute 10-Jahres Daten bezüglich Wirksamkeit und Sicherheit. Da Denosumab nicht über die Niere verstoffwechselt wird, wird es bevorzugt bei niereninsuffizienten Patienten eingesetzt. Aufgrund der potenten antiresorptiven Wirkung und des Hypokalzämie Risikos ist eine Kontrolle des Serumkalziums vor Therapiebeginn absolut indiziert. Auch unter Denosumab sind vereinzelt Osteonekrosen des Kiefers beschrieben. Nach Absetzen der Behandlung ist immer eine Anschlusstherapie, z.B. mit Alendronat oder Zoledronat indiziert, da es zu einem sogenannten Rebound Phänomen mit Anstieg der Knochenresorption, Mineralverlust und erhöhter Frakturrate kommen kann. Da dieses Rebound-Phänomen bei Patienten mit Vortherapie mit Bisphosphonaten seltener auftritt, wird Denosumab bevorzugt bei Patiennten nach erfolgter Bisphosphonattherapie eingesetzt.
Die intermittierende Gabe von N-terminalen 1-34 Fragment des Parathormons, bewirkt eine Stimulation der Osteoblasten und eine Zunahme der Knochenmasse, obwohl dauerhaft erhöhte Spiegel des intakten Parathormons 1-84 zu einem Knochenabbau führen.
Teriparatid (1-34 hPTH) ist eine osteoanabole Substanz mit nachgewiesener fraktursenkender Wirkung. Es wird täglich subkutan injiziert. Es war bislang, vor allem auf Grund der hohen Therapiekosten, als Reservemedikation für Fälle schwerer, manifester Osteoporose vorgesehen. Mittlerweile ist es als Generikum (Biosimilar) auf dem Markt.
Die Hormonersatztherapie (HRT) der postmenopausalen Frau bewirkt eine Reduktion der Knochenresorption und Zunahme der Knochendichte. Obwohl die fraktursenkende Wirkung der Östrogene gut belegt ist, empfehlen die Leitlinien in der Behandlung der Osteoporose eine HRT nur in Ausnahmefällen. Sie sollten aufgrund der pleiotropen Wirkungen nur bei Unverträglichkeit oder Kontraindikationen gegenüber anderen Osteoporosetherapeutika bzw. Frauen jünger als 65 mit Menopausensymptomen eingesetzt werden.